運動減輕血流再循環(huán)激活代謝轉(zhuǎn)能器 SCD1 催化血管保護性代謝物
Exercise mitigates flow recirculation and activates metabolic transducer SCD1 to catalyze vascular protective metabolites
KS:Exercise;flow recirculation;SCD1
作為對周期性心臟收縮的響應(yīng),血流在動脈循環(huán)中是脈動性的,脈動剪切應(yīng)力(PSS)是單向的,并且與血流方向?qū)R。PSS 促進血管保護性介質(zhì),包括內(nèi)皮一氧化氮合酶(eNOS)和超氧化物歧化酶(SOD),以減弱促炎細胞因子、粘附分子和還原型煙酰胺腺嘌呤二核苷酸磷酸(NADPH)氧化酶系統(tǒng)。相比之下,擾動的血流,包括振蕩剪切應(yīng)力 (OSS),在主動脈弓和動脈分叉處發(fā)展。OSS 是雙向的,并且與血流方向錯位,激活 NADPH 氧化酶以促進活性氧(ROS)。OSS 還誘導核因子κB(NF-κB)增加炎性細胞因子和血管細胞粘附分子1(VCAM1)。
體育鍛煉可增加循環(huán)系統(tǒng)中的血流,并調(diào)節(jié)分子轉(zhuǎn)導以改善代謝紊亂。在運動過程中,心肌收縮力和心率(HR)的增加會促進 PSS 改善內(nèi)皮可塑性,減輕動脈粥樣硬化形成,并延緩認知衰老和神經(jīng)退化。然而,特定運動激活的代謝傳感器在易紊亂血管系統(tǒng)中減輕氧化和炎癥的研究仍在進行中。
硬脂酰輔酶A去飽和酶1(SCD1)是位于線粒體相關(guān)內(nèi)質(zhì)網(wǎng)(ER)膜(MAMs)中的關(guān)鍵酶,它催化飽和脂肪酸(SFAs)轉(zhuǎn)化為 omega 9-單不飽和脂肪酸(MUFAs)。SCD1 的主要代謝物是油酸(OA)和棕櫚油酸(PA),它們分別由硬脂酸和棕櫚酸去飽和形成。據(jù)報道,雖然層流(穩(wěn)態(tài)和非脈動流)上調(diào)培養(yǎng)的人臍靜脈內(nèi)皮細胞中 PPARγ 依賴性 SCD1 表達,但最近,美國加州大學洛杉磯分校大衛(wèi)格芬醫(yī)學院心臟病學系、生物工程系研究團隊試圖證明自主轉(zhuǎn)輪跑步運動增強的 PSS 可減輕主動脈弓較小曲率中的血流再循環(huán),并激活內(nèi)皮 SCD1 以催化保護性代謝物。
為此,該團隊在動脈粥樣硬化小鼠模型(Ldlr-/-Scd1EC-/-)中使內(nèi)皮特異性缺失 SCD1 ,并接受高脂飲食(HFD)和自主輪式運動,對主動脈弓較小曲率的血流再循環(huán)進行了計算機模擬,并分析了 SCD1 介導的基因簇和抗炎代謝物的轉(zhuǎn)錄組學譜。研究表明,運動會增加時間-平均剪切應(yīng)力(τave)并降低較小曲率處的振蕩剪切指數(shù)(OSIave),且 PSS 激活 SCD1 作為代謝組學傳感器,以催化血管保護代謝物進行抗炎反應(yīng)。研究成果發(fā)表在Science Advances期刊題為“Exercise mitigates flow recirculation and activates metabolic transducer SCD1 to catalyze vascular protective metabolites”。
將人主動脈內(nèi)皮細胞(HAECs)暴露于動態(tài)流動系統(tǒng)中,非靶向代謝組學分析表明,PSS(50 dyne cm2,1 Hz)使 SCD1 催化的代謝物 OA 增加 2 倍,OSS(0.1 ± 4 dyne cm2,1 Hz)使其增加 1.3 倍。代謝物熱圖和主成分分析(PCA)均顯示 PSS 和 OSS 介導的代謝物與基礎(chǔ)水平分離。如前所述,PSS 進一步增加了糖酵解代謝物的產(chǎn)生。這些結(jié)果表明,PSS 激活內(nèi)皮 SCD1 以催化脂質(zhì)代謝物,這促使研究人員探索 PSS 是否會增加接受自主轉(zhuǎn)輪運動的小鼠的內(nèi)皮 SCD1 和隨后的血管保護。
CFD 模型顯示,在主動脈弓較小曲率處具有較低的時間-平均壁剪切應(yīng)力(TAWSS)和流動再循環(huán)。為了計算運動介導的 PSS 與 OSS,納入了 HR 和血流的變化。計算機分析表明,運動增強的 PSS 在較小曲率和較大曲率中均增加了 TAWSS,并在較小曲率中減輕了流動再循環(huán),而 OSIave 略有減少。這支持運動可調(diào)節(jié) TAWSS 和 OSIave,以減輕易血流紊亂的主動脈弓小曲率中的血流再循環(huán)。
為了證明運動介導的代謝物,在自主輪式跑步 24 小時之前和之后立即對雄性野生型 C57BL/6J 小鼠進行了非靶向代謝組學分析,發(fā)現(xiàn)運動后血漿 OA 顯著增加,PA 有增加趨勢。PCA 顯示,運動前后脂質(zhì)代謝物有明顯的分離。2 周后,主動脈內(nèi)皮的面部免疫染色顯示,SCD1 在主動脈弓的小曲率和降主動脈中的表達增加(圖1 B、C)。SCD1 染色在亞細胞核周區(qū)突出,但在 SCD1內(nèi)皮特異性缺失小鼠(Scd1EC-/-)中不存在。與 Scd1 特異性探針的原位雜交(RNAscope)證實了,運動后野生型小鼠主動脈弓和降主動脈中內(nèi)皮 SCD1 表達增加(圖1 E)。這些數(shù)據(jù)表明,運動增強的 PSS 與激活內(nèi)皮 SCD1 表達有關(guān)。
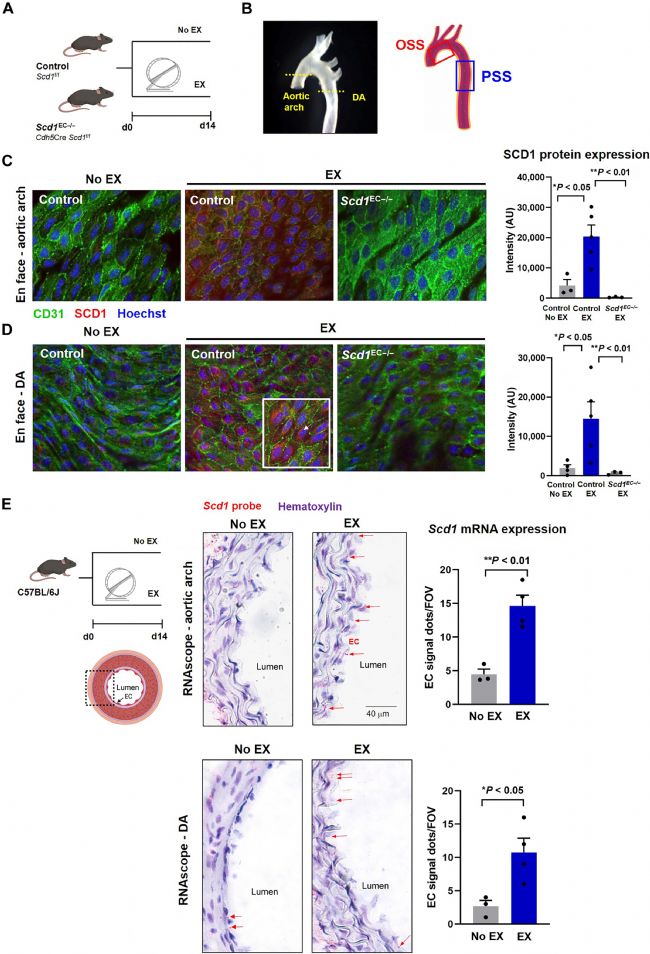 圖1 運動會激活內(nèi)皮 SCD1。
圖1 運動會激活內(nèi)皮 SCD1。
接下來,為了證明 SCD1 介導的代謝物對血管內(nèi)皮保護的作用,評估了致動脈粥樣硬化炎癥標志物。OA 處理降低了脂多糖(LPS)誘導的 HAECs 中 Vcam1、Icam1、Mcp1、Esel(E-選擇素)和 Cxcl8 趨化因子 mRNA 的表達 (圖2 A)。OA 還降低了 ER 應(yīng)激相關(guān)的轉(zhuǎn)錄因子,即 Atf3、Atf4 和 Atf6 mRNA 表達。
然后,通過基于腺病毒的重組系統(tǒng)過表達內(nèi)皮細胞 SCD1,以證明 Cxcl8 及其受體 Cxcr1 和嗅覺受體2(Or6a2)mRNA 表達的降低(圖2 B)。脂質(zhì)組學分析顯示,SCD1 過表達后,細胞內(nèi)組分和條件培養(yǎng)基中的 OA 濃度均增加(圖2 C)。PCA 分析顯示,與對照細胞相比,SCD1 過表達改變了脂質(zhì)組學特征,并增加了甘油三酯中的 MUFA 含量。過表達 SCD1 的 HAEC 條件培養(yǎng)基減輕了 LPS 誘導的 HAECs 中炎癥基因表達(圖2 D),表明細胞內(nèi)和細胞外 OA 都賦予抗炎反應(yīng)。
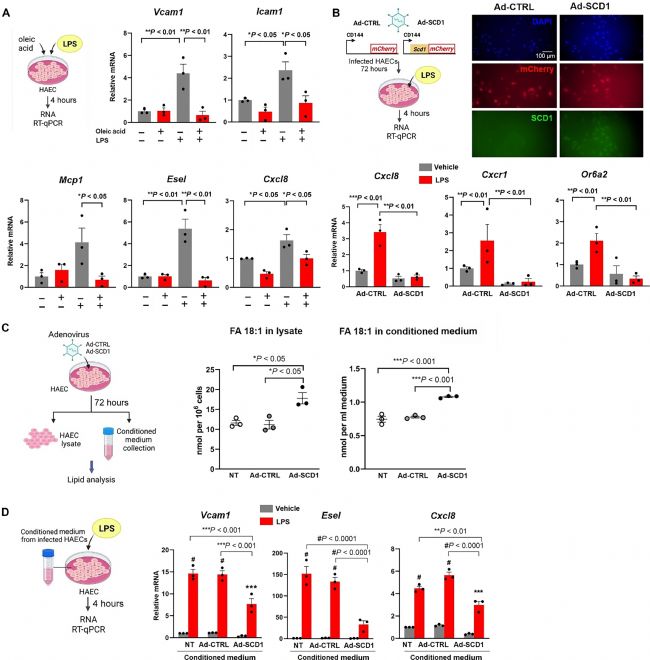 圖2 OA 處理或 SCD1 過表達減輕 HAEC 中的促炎介質(zhì)。
圖2 OA 處理或 SCD1 過表達減輕 HAEC 中的促炎介質(zhì)。
為了進一步證明 SCD1 介導的血管保護,構(gòu)建動脈粥樣硬化(Ldlr-/-)內(nèi)皮特異性缺失 SCD1小鼠模型(Ldlr-/- Scd1EC-/-),并喂食 HFD,14 天后,HFD 小鼠進行自主轉(zhuǎn)輪跑步(HFD-EX)。
第 28 天,靶向定量代謝組學分析顯示,與SCD1 沒有缺失的 Ldlr-/-Scd1 EC-/- 小鼠相比,久坐的 Ldlr-/-Scd1EC-/- 小鼠的循環(huán) OA 和 PA 基礎(chǔ)水平降低。運動組的 Ldlr-/-Scd1EC-/- 小鼠的血漿 OA 和 PA 水平與久坐組相似,而運動組的 Ldlr-/- 小鼠的 OA 和 PA 顯著升高。這些發(fā)現(xiàn)支持運動促進小鼠 SCD1 催化的血漿 OA 和 PA 水平的觀點。
計算機模擬顯示,運動增強的 PSS 減輕了沿主動脈弓較小曲率的血流再循環(huán)(圖3 A)。接下來,通過共聚焦顯微鏡對血管內(nèi)皮細胞 ETS-相關(guān)基因(ERG)核標記物和VCAM1粘附分子進行表面免疫染色。HFD 喂養(yǎng)的 Ldlr-/-小鼠受干擾血流暴露的小曲率中VCAM1 表達突出。HFD 喂養(yǎng)的 Ldlr-/-Scd1EC-/- 小鼠的 SCD1 缺失也產(chǎn)生了相似的 VCAM1 染色表達。然而,自主輪式運行 14 天減輕了 Ldlr -/- 小鼠中 VCAM1 的表達,但在 Ldlr -/- Scd1EC-/- 小鼠中沒有降低(圖3 A、C)。
在內(nèi)皮暴露于 PSS 的降主動脈中(圖3 B)未觀察到 VCAM1 表達。共聚焦成像證實了 HFD 喂養(yǎng)的 Ldlr -/- 小鼠降主動脈中少量的 VCAM1 陽性細胞,而內(nèi)皮 Scd1 (Ldlr -/- Scd1EC-/-)的缺失增加了 VCAM1 陽性細胞的數(shù)量。此外,14 天的自主運動并未減少 Ldlr-/- Scd1EC-/- 小鼠中 VCAM1 陽性內(nèi)皮細胞(圖3 B、C)。
運動后,Ldlr-/- 小鼠在主動脈弓的受干擾血流區(qū)域產(chǎn)生了明顯的 SCD1 染色,這在 Ldlr-/-Scd1EC-/- 小鼠中不存在,與 SCD1 特異性探針(RNAscope)的原位雜交證明了這一點(圖3 E)。因此,運動增強的 PSS 激活內(nèi)皮 SCD1 以減少粘附分子的表達。
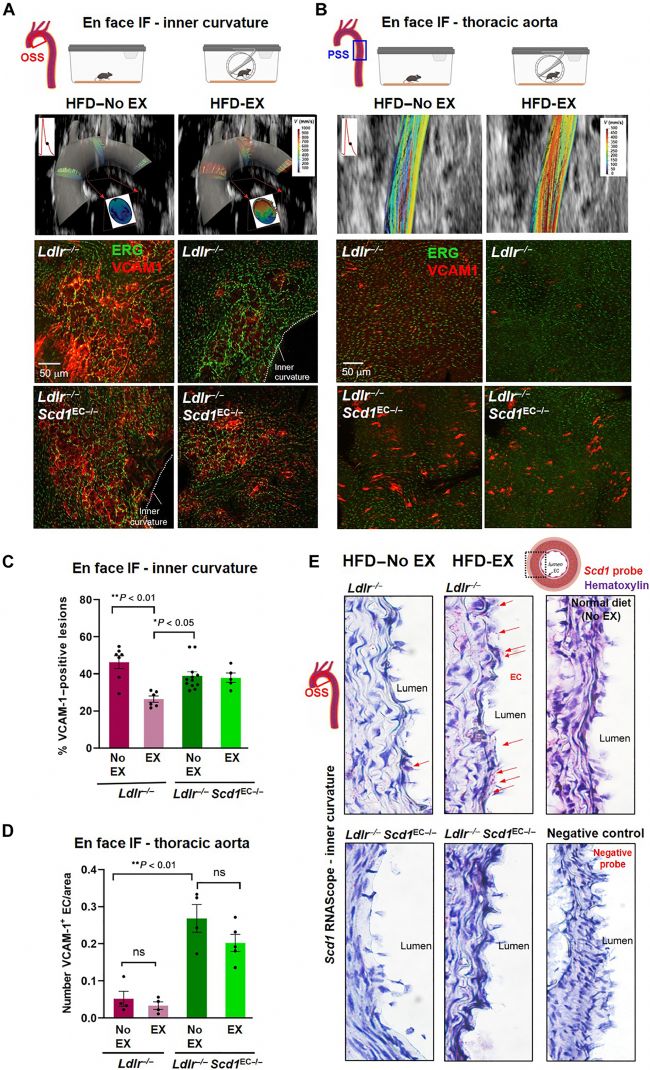 圖3 內(nèi)皮特異性 Scd1 缺失消除了運動介導的抗炎介質(zhì)。
圖3 內(nèi)皮特異性 Scd1 缺失消除了運動介導的抗炎介質(zhì)。
最后,對經(jīng)歷三種情況的 Ldlr-/- 小鼠的主動脈進行了單細胞 RNA 測序:(i)正常食物飲食,(ii)HFD 和(iii)HFD-EX,確定了一個明確的內(nèi)皮亞簇,其中較高水平的 Pparγ 和 Scd1 與較高水平的 Vcam1 表達相關(guān)。大多數(shù) Vcam1 表達較高的內(nèi)皮細胞與 HFD 相關(guān)。通過將內(nèi)皮轉(zhuǎn)錄組數(shù)據(jù)與已發(fā)布的數(shù)據(jù)庫整合,發(fā)現(xiàn)與內(nèi)皮 Scd1 相互作用的潛在候選基因,包括脂聯(lián)素受體2(Adipor2)、過氧化物酶體酰基輔酶 A 氧化酶 1(Acox1)和胰島素受體底物2(Irs2)。
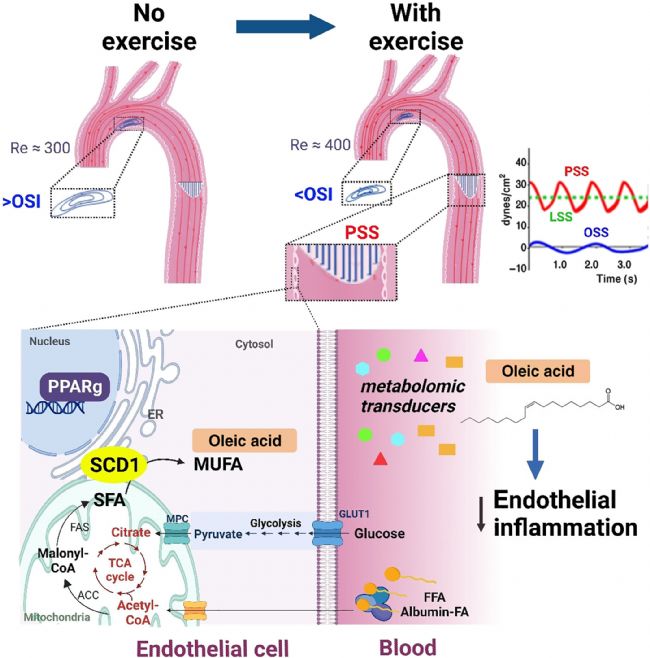 圖4 主動脈中運動增強的 PSS 和動脈粥樣硬化保護代謝物的血流響應(yīng)性 PPARγ-SCD1 通路的激活示意圖模型。
圖4 主動脈中運動增強的 PSS 和動脈粥樣硬化保護代謝物的血流響應(yīng)性 PPARγ-SCD1 通路的激活示意圖模型。
運動減輕主動脈弓中的血流再循環(huán)和 OSI。位于 ER 膜中的 SCD1 催化 SFA 轉(zhuǎn)化為 MUFA,導致細胞內(nèi)和循環(huán)中 OA 的水平增加。OA 抑制 NF-κB 介導的內(nèi)皮炎癥標志物。
總之,該研究表明,運動增強的 PSS 激活內(nèi)皮 SCD1 以催化血管保護性脂質(zhì)代謝物 OA 和 PA。雖然 SCD1 與跨組織代謝相關(guān),但研究揭示了內(nèi)皮特異性 SCD1 可減輕受干擾血流暴露的主動脈弓中的炎癥反應(yīng)。總體而言,遺傳小鼠模型的整合、自主運動和計算機分析提供了對血流響應(yīng) SCD1 作為代謝轉(zhuǎn)導以減輕心臟代謝紊亂的見解。
參考文獻:Cavallero S, Roustaei M, Satta S, Cho JM, Phan H, Baek KI, Blázquez-Medela AM, Gonzalez-Ramos S, Vu K, Park SK, Yokota T, Sumner J, Mack JJ, Sigmund CD, Reddy ST, Li R, Hsiai TK. Exercise mitigates flow recirculation and activates metabolic transducer SCD1 to catalyze vascular protective metabolites. Sci Adv. 2024 Feb 16;10(7):eadj7481. doi: 10.1126/sciadv.adj7481. Epub 2024 Feb 14. PMID: 38354249; PMCID: PMC10866565.
原文鏈接:https://pubmed.ncbi.nlm.nih.gov/38354249/
IF:11.7
ISSN:2375-2548
圖片來源: 所有圖片均來源于參考文獻
小編旨在分享、學習、交流生物科學等領(lǐng)域的研究進展。如有侵權(quán)或引文不當請聯(lián)系小編修正。如有任何的想法以及建議,歡迎聯(lián)系小編。感謝各位的瀏覽以及關(guān)注!進入官網(wǎng)www.naturethink.com或關(guān)注“Naturethink”公眾號,了解更多相關(guān)內(nèi)容。
點擊了解:流體剪切力系統(tǒng)
- 運動減輕血流再循環(huán)激活代謝轉(zhuǎn)能器 SCD1 催化血管保護性代謝物
- ASD地物光譜儀在快速檢測沙丁魚新鮮度方面的應(yīng)用
- 靶向軟骨下骨骨細胞中的H19用于減輕骨關(guān)節(jié)炎軟骨降解
- 內(nèi)皮雌激素-心肌cGMP軸決定壓力超負荷期間的血管生成和心臟功能
- 機械拉伸誘導的活性氧驅(qū)動新生豬腎上皮細胞內(nèi)皮素的產(chǎn)生
- Hes1/Piezo1 通路在糖皮質(zhì)激素誘導的骨質(zhì)疏松癥中的關(guān)鍵作用
- 文獻解讀:用二次諧波色散掃描表征超短激光脈沖
- 如何選擇和使用飛秒脈沖測量和壓縮器d-scan系列產(chǎn)品